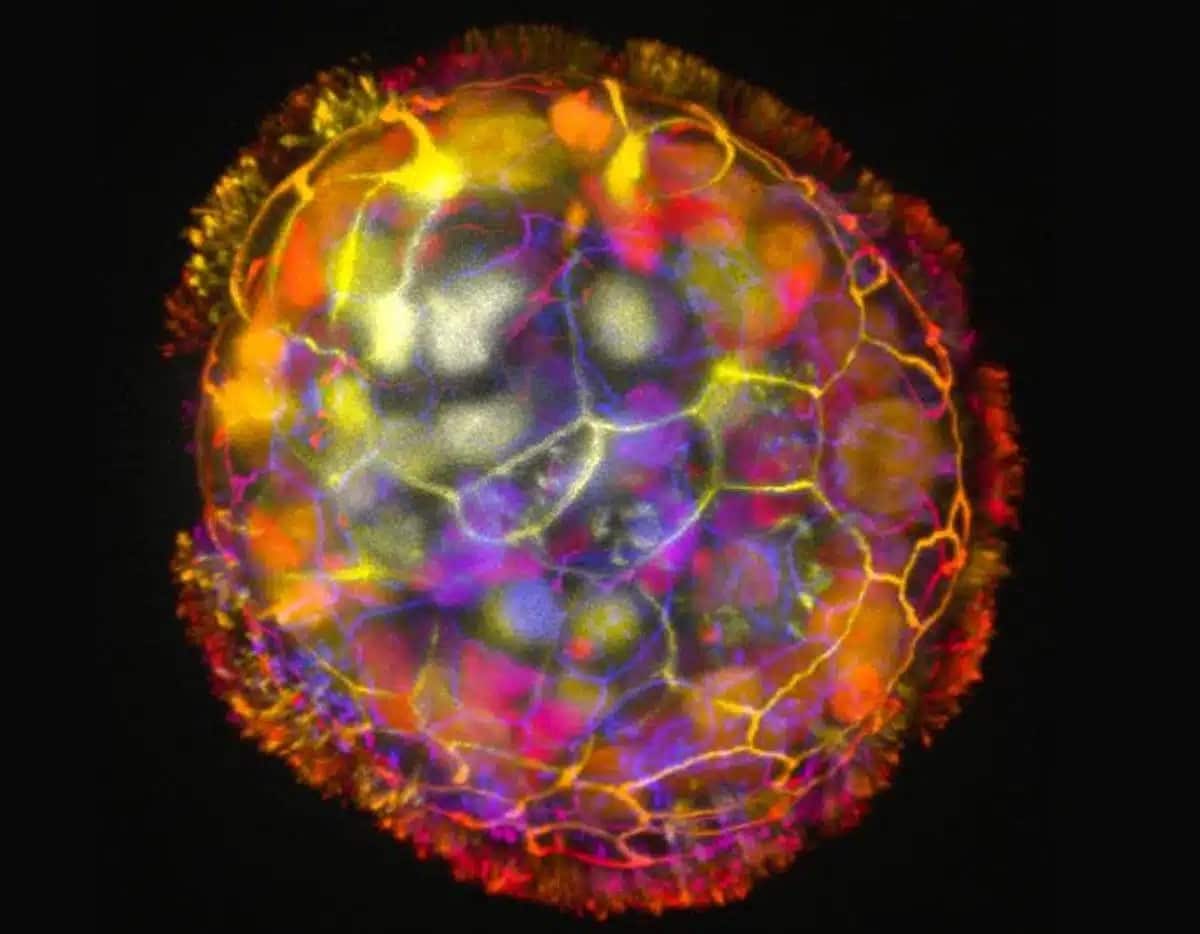
Los investigadores están revolucionando la medicina regenerativa con ‘Anthrobots’, robots biológicos creados a partir de células traqueales humanas que prometen nuevas formas de curación y tratamiento
Los investigadores de la Universidad de Tufts y el Instituto Wyss de la Universidad de Harvard han desarrollado «Anthrobots», pequeños robots biológicos creados a partir de células traqueales humanas. Estos robots multicelulares, cuyo tamaño varía desde el ancho de un cabello humano hasta la punta de un lápiz afilado, tienen la capacidad de autoensamblarse y han demostrado un efecto curativo notable en otras células. Este descubrimiento abre el camino para utilizar biobots derivados de pacientes como nuevas herramientas terapéuticas para la regeneración, la curación y el tratamiento de enfermedades.
El trabajo se basa en investigaciones anteriores en las que se crearon robots biológicos multicelulares a partir de células embrionarias de ranas, conocidos como «Xenobots». Sin embargo, en este nuevo estudio, publicado en «Advanced Science», se descubrió que los bots también pueden crearse a partir de células humanas adultas sin modificación genética, mostrando algunas capacidades más allá de las observadas con los Xenobots. Esto comienza a responder preguntas sobre las reglas que rigen cómo se ensamblan y trabajan juntas las células en el cuerpo, y si se pueden reorganizar en diferentes «planes corporales» para llevar a cabo otras funciones.
Los investigadores dieron a las células humanas la oportunidad de reiniciarse y encontrar formas de crear nuevas estructuras y tareas. Se descubrió que estas células no solo podían crear nuevas formas multicelulares, sino que también podían moverse de diferentes maneras sobre una superficie de neuronas humanas cultivadas en un plato de laboratorio y fomentar un nuevo crecimiento para llenar los huecos causados por rasguños en la capa de células.
Los robots que se ensamblan a sí mismos
Levin, director del Allen Discovery Center en Tufts y miembro asociado del Wyss Institute, destacó que las ventajas de usar células humanas incluyen la capacidad de construir bots a partir de las propias células del paciente para realizar trabajos terapéuticos sin el riesgo de desencadenar una respuesta inmune o requerir inmunosupresores. Además, los Anthrobots solo pueden sobrevivir en condiciones de laboratorio muy específicas, por lo que no hay riesgo de exposición o propagación no deseada fuera del laboratorio. Tampoco se reproducen y no tienen ediciones genéticas, adiciones o eliminaciones, por lo que no hay riesgo de que evolucionen más allá de las salvaguardias existentes.
Estos Anthrobots se autoensamblan en el plato de laboratorio y, a diferencia de los Xenobots, no requieren pinzas o escalpelos para darles forma, y se pueden usar células adultas, incluso de pacientes mayores, en lugar de células embrionarias. Esto es totalmente escalable, y se pueden producir enjambres de estos bots en paralelo, lo que es un buen comienzo para desarrollar una herramienta terapéutica.
En pruebas de laboratorio, los Anthrobots sin modificaciones genéticas provocaron un regrowth sustancial, creando un puente de neuronas tan grueso como el resto de las células sanas en el plato. Según los investigadores, el desarrollo adicional de los bots podría llevar a otras aplicaciones, incluyendo la limpieza de la acumulación de placa en las arterias de pacientes con aterosclerosis, la reparación de daños en la médula espinal o los nervios de la retina, el reconocimiento de bacterias o células cancerosas o la entrega de medicamentos a tejidos específicos.
Gumuskaya explicó que las células tienen la capacidad innata de autoensamblarse en estructuras más grandes de ciertas maneras fundamentales, lo que ayuda a los científicos a construir los bots y también a comprender cómo se ensamblan los planes corporales naturales, cómo el genoma y el medio ambiente trabajan juntos para crear tejidos, órganos y extremidades, y cómo restaurarlos con tratamientos regenerativos.
REFERENCIA
Motile Living Biobots Self-Construct from Adult Human Somatic Progenitor Seed Cells