Investigadores de la Universidad de Virginia y el Mount Sinai identifican en la revista Circulation el mecanismo molecular que explica por qué más de la mitad de los pacientes con enfermedad renal crónica mueren de problemas cardiovasculares.
Uno de cada siete adultos tiene enfermedad renal crónica sin saberlo. Y durante décadas, los médicos sabían que estas personas morían con una frecuencia alarmante de infarto o insuficiencia cardiaca, pero no entendían bien por qué. Ahora lo saben. Los riñones dañados producen unas partículas que viajan por la sangre hasta el corazón y lo envenenan de forma silenciosa.
El mensajero que se convierte en asesino
Las células de nuestro organismo se comunican constantemente entre sí mediante pequeñas vesículas extracelulares: partículas microscópicas que actúan como paquetes de mensajería, transportando proteínas y material genético de un órgano a otro. En condiciones normales, este sistema es esencial para el funcionamiento del cuerpo. Pero el equipo dirigido por Uta Erdbrügger, médica e investigadora de la División de Nefrología de la Universidad de Virginia, ha descubierto que en los riñones enfermos este mecanismo se pervierte.
Las vesículas extracelulares producidas por riñones con enfermedad renal crónica (ERC) no llevan mensajes útiles. Llevan moléculas de ARN pequeño (miARN) que son directamente tóxicas para el músculo cardiaco. Cuando estas partículas llegan al corazón a través del torrente sanguíneo, alteran su funcionamiento y aceleran el desarrollo de insuficiencia cardiaca. El estudio, publicado en la revista Circulation con acceso abierto, es la primera demostración de un factor de riesgo específico del riñón que explica el daño cardiaco.
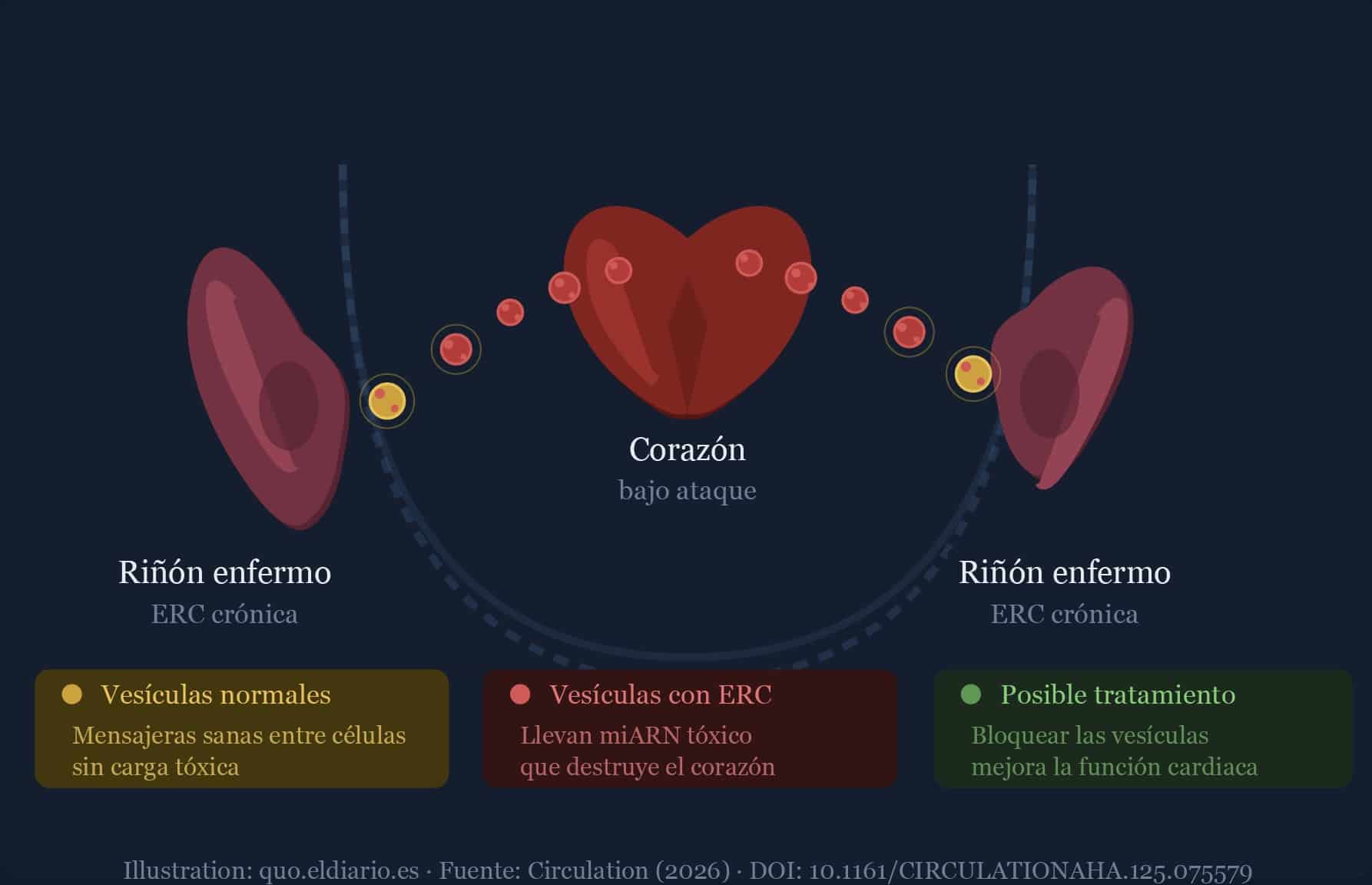
Así afectan los riñones con enfermedad renal crónica al corazón. Imagen generada en parte mediante IA.
Ratones bloqueados, corazones recuperados
Para confirmar que estas vesículas eran efectivamente la causa y no una consecuencia del problema, los investigadores realizaron experimentos en ratones con enfermedad renal. Cuando bloquearon la circulación de las vesículas extracelulares patológicas, la función cardiaca mejoró de forma significativa y los síntomas de insuficiencia cardiaca se aliviaron. El experimento inverso también funcionó: al inyectar las vesículas de pacientes humanos con ERC en ratones sanos, el corazón de los animales comenzó a deteriorarse.
Los investigadores analizaron también muestras de plasma sanguíneo de pacientes con enfermedad renal crónica y de donantes sanos, y confirmaron que las vesículas tóxicas estaban presentes exclusivamente en los pacientes enfermos. «Los médicos siempre se preguntaron cómo se comunican entre sí órganos como el riñón y el corazón. Demostramos que las vesículas del riñón pueden viajar hasta el corazón y resultar tóxicas», explicó Erdbrügger. «Solo estamos empezando a entender esta comunicación».
Un misterio médico con nombre y apellidos
La conexión entre la enfermedad renal crónica y los problemas cardiovasculares lleva documentada décadas. Más de la mitad de los pacientes con ERC mueren de complicaciones cardiacas, no de fallo renal. La gravedad del daño al corazón crece en paralelo a la del deterioro renal. Pero hasta ahora, nadie había podido señalar un mecanismo causal específico del riñón: la diabetes, la hipertensión y la obesidad, presentes en muchos de estos pacientes, enturbiaban el análisis. El descubrimiento de estas vesículas extracelulares patológicas despeja esa confusión.
«La enfermedad renal y la cardiaca pueden progresar en silencio, y a menudo solo se descubren cuando el daño ya está hecho», reconoció Erdbrügger. «Nuestros hallazgos pueden ayudar a identificar antes a los pacientes en riesgo de insuficiencia cardiaca, lo que permitiría tratamientos más tempranos y mejores resultados». En España, donde la prevalencia de la ERC en adultos mayores de 64 años supera el 20%, este tipo de herramienta diagnóstica tiene un potencial enorme.
El horizonte: una analítica de sangre que salve el corazón
Los investigadores ya trabajan en dos aplicaciones prácticas de su hallazgo. La primera es el desarrollo de un biomarcador en sangre que permita detectar qué pacientes con enfermedad renal tienen mayor riesgo de sufrir insuficiencia cardiaca antes de que aparezcan los síntomas. La segunda, más ambiciosa, es diseñar un tratamiento que bloquee o neutralice las vesículas tóxicas antes de que lleguen al corazón, una especie de antídoto molecular para el veneno renal.
El laboratorio de Erdbrügger ya ha organizado un taller intensivo de cinco días en la Universidad de Virginia para formar a otros investigadores en el trabajo con vesículas extracelulares, lo que indica que este campo está madurando rápido. «Nuestra esperanza es desarrollar nuevos biomarcadores y opciones de tratamiento para los pacientes renales en riesgo de enfermedad cardiaca», dijo. El trabajo, financiado por los Institutos Nacionales de Salud de Estados Unidos, abre una vía terapéutica que hasta hace muy poco parecía ciencia ficción: interceptar los mensajes que un órgano enfermo manda a otro para detener el daño antes de que sea irreversible.
REFERENCIA