Publicadas las primeras imágenes tridimensionales de la sinapsis inmunológica, la diminuta zona de contacto ultraorganizada que los linfocitos T citotóxicos forman para destruir células cancerosas sin atacar a las células vecinas
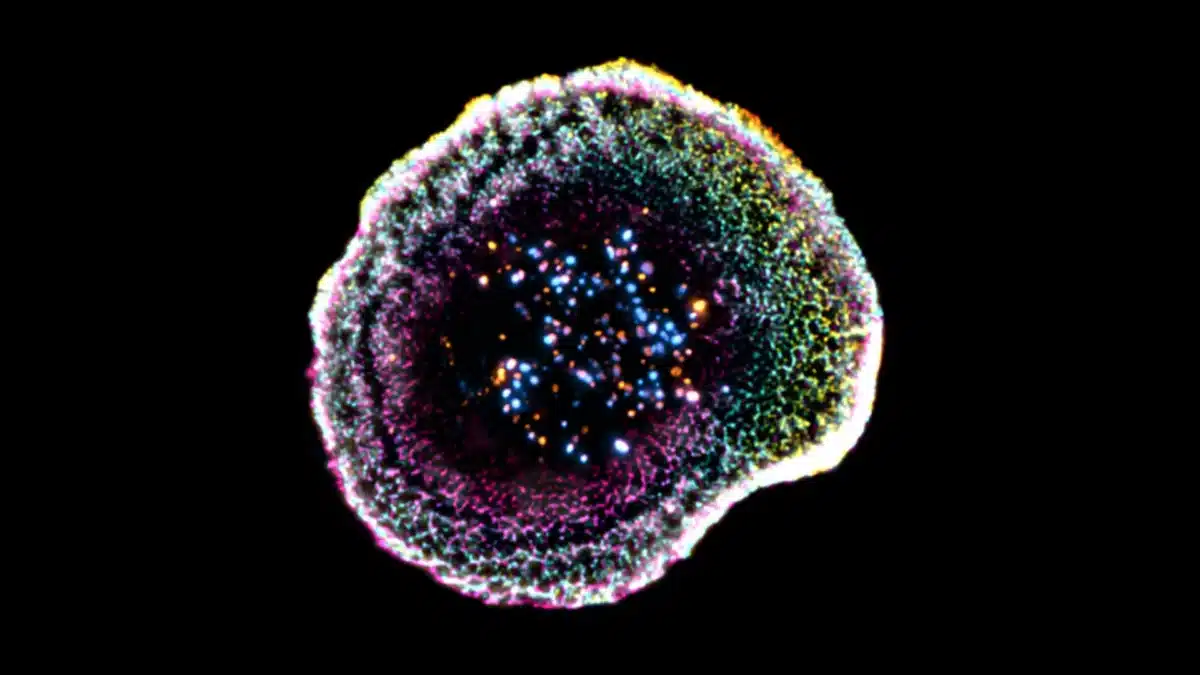
Imagen; una célula T citotóxica captada mediante microscopía de criocontracción (cryo-ExM). Los puntos de colores que se observan en el centro son gránulos citotóxicos que se utilizan para destruir células infectadas o cancerosas. © F. Lemaitre @ UNIGE
El sistema inmune tiene asesinos a sueldo, se llaman linfocitos T citotóxicos o células T asesinas (killer cells). Su trabajo es localizar y eliminar células infectadas o cancerosas. Lo hacen mediante un mecanismo extraordinariamente preciso que los científicos conocían en sus líneas generales, pero que nunca habían podido ver con nitidez hasta ahora.
Un equipo de la Universidad de Ginebra ha desarrollado una técnica llamada cryo-expansion microscopy (cryo-ExM) que por primera vez permite fotografiar en tres dimensiones la arquitectura molecular exacta de la sinapsis inmunológica: el punto de contacto entre el linfocito T y la célula que va a matar.
La sinapsis inmunológica: un andamio molecular para una ejecución
Cuando un linfocito T reconoce una célula cancerosa, no simplemente le dispara toxinas al azar. Forma una estructura de contacto altamente organizada llamada sinapsis inmunológica. Aquí las proteínas se disponen en capas concéntricas con una geometría casi perfecta. En el centro se concentran los receptores que reconocen a la célula enemiga. Alrededor, en un anillo, se sitúan las moléculas de adhesión que mantienen el contacto; en el perímetro exterior, las proteínas de señalización. Esta arquitectura permite a la célula T dirigir sus «cargas» letales (perforinas y granzimas) exactamente hacia la célula diana, sin que escapen hacia el tejido circundante.
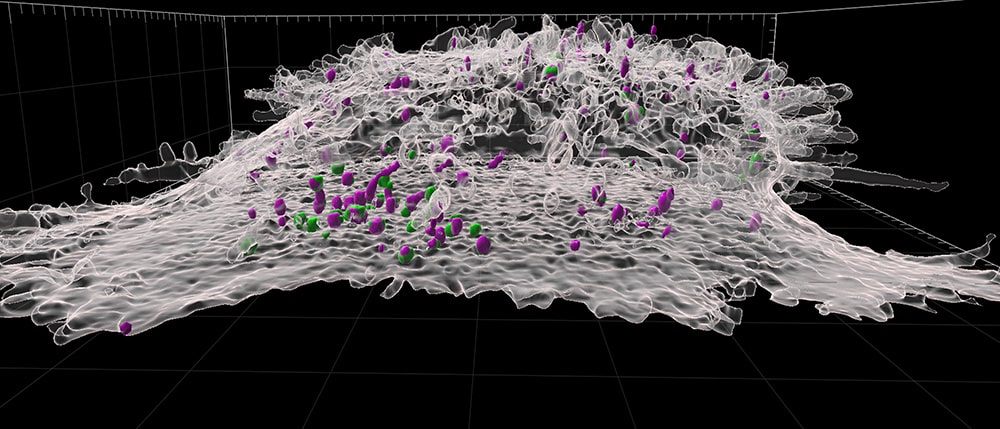
Reconstrucción en 3D de una célula T CD8 activada, fijada criogénicamente y expandida. La imagen muestra la membrana plasmática en gris transparente y los gránulos líticos que contienen granzima B en verde y perforina en magenta. © F. Lemaitre @ UNIGE
El problema era que hasta ahora no existía ninguna técnica capaz de visualizar esa arquitectura con resolución nanométrica en un tejido tridimensional real. Los métodos de microscopía convencionales bidimensionales habían dado pistas, pero no la imagen completa. La cryo-ExM desarrollada por el equipo de Virginie Hamel, Paul Guichard y Benita Wolf en Ginebra combina la expansión física del tejido (que separa las moléculas lo suficiente como para verlas individualmente) con la microscopía crioelectrónica de alta resolución.
El resultado son imágenes en las que cada proteína de la sinapsis inmunológica aparece localizada con una precisión de nanómetros. Para hacerse una idea, los átomos tienen entre 0,1 y 0,5 nanometros de diámetro.
Lo que revelan las imágenes en 3D
Las primeras imágenes 3D completas de la sinapsis inmunológica publicadas en Cell Reports confirman y amplían la arquitectura conocida, pero también revelan detalles inesperados. Las perforinas, las proteínas que literalmente perforan la membrana de la célula diana para introducir las granzimas que la matarán, se organizan en estructuras semiesféricas que apuntan exclusivamente hacia la célula objetivo. Esta geometría explica por qué el linfocito T puede matar con tanta precisión sin generar daño colateral: las toxinas viajan en una dirección definida por la arquitectura tridimensional de la sinapsis.
«Ahora podemos ver el andamio molecular completo que orquesta la respuesta inmune», señaló Benita Wolf, una de las autoras principales. «Esto no es solo un avance científico básico: abre la posibilidad de diseñar células T mejoradas para inmunoterapia que formen sinapsis más eficientes o más precisas».
Lo que significa para los pacientes de cáncer
La inmunoterapia basada en células T (incluyendo las terapias CAR-T, en las que se extraen linfocitos del paciente, que se modifican genéticamente para reconocer mejor el tumor y se reinfunden) es uno de los campos más prometedores de la oncología actual.
En España, los primeros tratamientos CAR-T fueron aprobados en 2019 para leucemias y linfomas, y su uso se ha extendido en los últimos años. Uno de los problemas que limita su eficacia es que las células T modificadas a veces forman sinapsis defectuosas con las células tumorales, lo que reduce su capacidad de matar. Tener ahora un mapa 3D completo de cómo debería verse una sinapsis eficiente abre la posibilidad de optimizar esas células para que sus sinapsis modificadas se parezcan más al ideal biológico. Es, en esencia, disponer de los planos del arma perfecta.
REFERENCIA